11 octobre 2019 -- Le congrès national de radiologie (JFR) a débuté avec une focalisation accrue sur l'intelligence artificielle (IA) et l'apprentissage automatique. La discussion comprenait une mise à jour d'un projet ambitieux visant à créer un écosystème national en France pour le développement d'algorithmes.
S'exprimant lors de la séance pédagogique "IA: Quelle dynamique en 2019?" Le Pr Jean-Paul Beregi, responsable de l'imagerie à l'hôpital universitaire de Nȋmes, a informé les délégués sur l'état actuel de la nouvelle initiative d'imagerie française DRIM France IA, un écosystème d'IA indépendant et à but non lucratif.
Le projet a considérablement progressé depuis son annonce en octobre dernier, selon le Pr Beregi. L'écosystème a maintenant un comité scientifique et une charte, et cherche des moyens d'aller de l'avant avec les partenaires institutionnels.
"Nous sommes maintenant en mesure d'évaluer les rôles et les contributions d'autres acteurs", a déclaré le Pr Beregi.
Nous espérons que DRIM France sera suffisamment établi pour servir de plate-forme de test neutre pour les start-ups privées ou les hôpitaux publics souhaitant valider leurs algorithmes sur une base de données concrète dès 2020, selon le Pr Beregi.
De plus, DRIM France devrait jouer un rôle plus important dans le Big Data Challenge de JFR 2020 l'année prochaine, dans le but d'élargir la compétition pour inclure l'impact de l'IA sur des questions relatives non seulement à la pathologie mais également à la dose, à la pertinence et au pronostic. Les équipes auront accès à d'autres informations non liées à l'image, notamment l'indication clinique, la biologie, la dose absorbée, et les antécédents du patient extraits de RIS et de PACS.
L'événement de cette année a débuté le vendredi avec 18 équipes qui avaient jusqu'à dimanche soir pour soumettre leurs conclusions en utilisant leurs propres algorithmes. Cette année, la base de données contenait 4 500 images CT et IRM sur les trois thèmes suivants: nodules pulmonaires, sclérose en plaques et sarcopénie.
Les gagnants 2019:
- Pour le nodule pulmonaire : IBM France cognitive
- Pour la sarcopénie : Owkin
- Pour la sclérose en plaque : Pixyl (start-up crée par l'INSERM et l'INRIA il y a 4 ans) avec le concours de neuroradiologues du groupement des hôpitaux de l'institut catholique de Lille et de l'institut des neurosciences de Grenoble



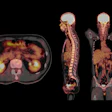
![Overview of the study design. (A) The fully automated deep learning framework was developed to estimate body composition (BC) (defined as subcutaneous adipose tissue [SAT] in liters; visceral adipose tissue [VAT] in liters; skeletal muscle [SM] in liters; SM fat fraction [SMFF] as a percentage; and intramuscular adipose tissue [IMAT] in deciliters) from MRI. The fully automated framework comprised one model (model 1) to quantify different BC measures (SAT, VAT, SM, SMFF, and IMAT) as three-dimensional (3D) measures from whole-body MRI scans. The second model (model 2) was trained to identify standardized anatomic landmarks along the craniocaudal body axis (z coordinate field), which allowed for subdividing the whole-body measures into different subregions typically examined on clinical routine MRI scans (chest, abdomen, and pelvis). (B) BC was quantified from whole-body MRI in over 66,000 individuals from two large population-based cohort studies, the UK Biobank (UKB) (36,317 individuals) and the German National Cohort (NAKO) (30,291 individuals). Bar graphs show age distribution by sex and cohort. BMI = body mass index. (C) After the performance assessment of the fully automated framework, the change in BC measures, distributions, and profiles across age decades were investigated. Age-, sex-, and height-adjusted body composition reference curves were calculated and made publicly available in a web-based z-score calculator (https://circ-ml.github.io).](https://img.auntminnieeurope.com/mindful/smg/workspaces/default/uploads/2026/05/body-comp.XgAjTfPj1W.jpg?auto=format%2Ccompress&fit=crop&h=100&q=70&w=100)

![Overview of the study design. (A) The fully automated deep learning framework was developed to estimate body composition (BC) (defined as subcutaneous adipose tissue [SAT] in liters; visceral adipose tissue [VAT] in liters; skeletal muscle [SM] in liters; SM fat fraction [SMFF] as a percentage; and intramuscular adipose tissue [IMAT] in deciliters) from MRI. The fully automated framework comprised one model (model 1) to quantify different BC measures (SAT, VAT, SM, SMFF, and IMAT) as three-dimensional (3D) measures from whole-body MRI scans. The second model (model 2) was trained to identify standardized anatomic landmarks along the craniocaudal body axis (z coordinate field), which allowed for subdividing the whole-body measures into different subregions typically examined on clinical routine MRI scans (chest, abdomen, and pelvis). (B) BC was quantified from whole-body MRI in over 66,000 individuals from two large population-based cohort studies, the UK Biobank (UKB) (36,317 individuals) and the German National Cohort (NAKO) (30,291 individuals). Bar graphs show age distribution by sex and cohort. BMI = body mass index. (C) After the performance assessment of the fully automated framework, the change in BC measures, distributions, and profiles across age decades were investigated. Age-, sex-, and height-adjusted body composition reference curves were calculated and made publicly available in a web-based z-score calculator (https://circ-ml.github.io).](https://img.auntminnieeurope.com/mindful/smg/workspaces/default/uploads/2026/05/body-comp.XgAjTfPj1W.jpg?auto=format%2Ccompress&fit=crop&h=112&q=70&w=112)